生物工程学院王贵学教授团队研究论文在《Advanced Science》在线发表
近日,我校生物工程学院王贵学教授团队的实验研究论文“Biomimetic Nanotherapies: Red Blood Cell d Core–Shell Structured Nanocomplexes for Atherosclerosis Management” 在国际权威学术期刊《Advanced Science》(最新影响因子12.441)在线发表(DOI: 10.1002/advs.201900172),该论文第一作者为2015级博士研究生王溢,通讯作者为王贵学教授,青年教师吴伟副教授为共同通讯作者,重庆大学为该论文的第一完成单位和通讯作者单位。
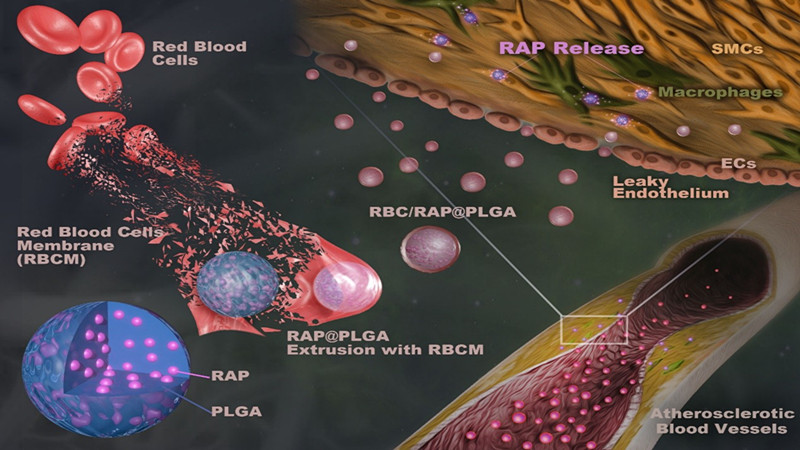
仿生纳米药物RBC/RAP@PLGA的制备及治疗AS示意图
动脉粥样硬化(Atherosclerosis, AS)是一种典型的慢性炎症性血管病变,是脑血管病、冠心病和外周动脉疾病等缺血性心脑血管病的共同病理学基础,严重危害人类健康。目前,临床上常采用口服降脂或抗炎药物来抑制AS的发生发展,然而传统的口服药物治疗存在利用率低、见效慢、毒副作用严重等问题。纳米药物递送系统能够增溶药物、提高药物半衰期、改善药物体内分布、降低毒副作用,在临床AS诊断和治疗中具有极大的应用价值和广阔的市场前景。但是,传统的纳米药物递送系统难以被正常的生物机体交互认可,不可避免地被作为“非己”异物被机体清除,难以靶向输送药物到靶病变部位。
基于以上问题,王贵学教授团队创新地通过协同“自体”与“人工”药物递送系统的仿生设计策略,将红细胞(RBC)包被于纳米药物RAP@PLGA上,构建了具备药物缓释、长效血液循环及高效靶向AS药物递送功能的仿生纳米药物RBC/RAP@PLGA,并首次用于AS的治疗。研究结果表明:该仿生纳米药物能够在小鼠模型中实现AS的安全、高效治疗。本研究为AS的纳米药物治疗提供一种新的设计思路,有助于个体化及精准化AS治疗的发展,具有重要的科学研究意义及潜在的临床应用价值。
该研究工作得到了“十三五”国家重点研发计划项目(2016YFC1102305)、国家自然科学基金(51603023,11572064)及中央高校研究基金和重庆市基础科学与前沿技术研究专项的部分支持。英国格拉斯哥大学Sean McGinty博士,意大利应用数学研究所Giuseppe Pontrelli博士参与了药物释放模拟研究与论文编辑。美国哈佛大学医学院Jun Ren博士、Qiwei Wang博士参与了结果分析与论文编辑。
(论文详情请点击:https://onlinelibrary.wiley.com/doi/full/10.1002/advs.201900172 )
 我要投稿
我要投稿
